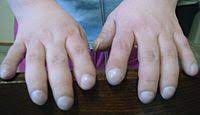
Муковісцидоз (МВ) – аутосомно-рецесивне захворювання, зумовлене мутаціями в гені CFTR (cystic fibrosis transmembrane conductance regulator), що призводять до порушення транспорту іонів хлору та натрію через клітинну мембрану, спричиняють дегідратацію апікальної поверхні секреторного епітелію та збільшення в'язкості слизу.<МВ уражає дихальні шляхи, шлунково-кишковий тракт, печінку, підшлункову залозу, слинні, потові залози, репродуктивну систему.
Це одне з найпоширеніших спадкових захворювань з частотою народження 1 на 4500 осіб, при цьому частота носія мутацій гена CFTR досягає 1 на 25 осіб. Ще у 50-ті роки минулого сторіччя МВ відносили до розряду «фатальних захворювань», оскільки 60 % хворих помирали у віці до 1 року. Сьогодні завдяки розширенню знань про захворювання та спеціалізованій медичній допомозі МВ перейшов у розряд хронічних, а медіана очікуваної тривалості життя у розвинених країнах перевищила 45-річний рубіж.
Стрімкий розвиток медичної науки та накопичений досвід за останнє десятиліття змінили підходи до діагностики та терапії МВ:
- ДНК-діагностика (вид мутації дозволяє прогнозувати клінічний перебіг захворювання, ДНК-діагностика частих мутацій та секвенування гена визначають вибір етіопатогенетичного препарату).
- Комп'ютерна томографія дає можливість точно діагностувати обсяг та вид ураження легеневої тканини, що визначає вибір терапії.
- Мікробіологічна діагностика та моніторинг виду та типу мікробного збудника, його резистентності до антимікробної терапії дозволяють індивідуалізувати призначення антибактеріального препарату.
З появою у 2012 році таргетних препаратів розкрито нові можливості персоналізованого підходу до терапії хворих на МВ. У теперішній час у світі використовується чотири таргетні препарати, які модулюють (потенціюють і коригують) білок CFTR. Серед таких препаратів «Калідеко» (Kalydeco, івакафтор), «Оркамбі» (Orcambi, люмакавтор + івакавтор), Сімдеко (Symdeco, тезакафтор+ивакафтор) та «Трикафта» або «Кафтрио» (Trikafta, елексакафтор + тезакафтор + івакафтор, івакафтор). Розроблені препарати стали новими кроком у терапії МВ, вони дозволили підвищити якість життя хворих та її тривалість. Дослідження в області етіологічної та патогенетичної терапії МВ на сьогоднішній день продовжуються (https://cysticfibrosisnewstoday.com/cystic-fibrosis-therapy-tracker/).
Інформація надана кафедрою пропедевтики дитячих хвороб